可编程 RNA 编辑工具能够对突变转录本进行可逆校正,从而降低与使用 DNA 编辑工具相关的永久性遗传变化相关的潜在风险。然而,这些 RNA 工具治疗疾病的潜力仍然未知。
2022年7月20日,复旦大学舒易来,李华伟及中国科学院脑科学与智能技术卓越创新中心杨辉共同通讯在Science Translational Medicine 在线发表题为“Rescue of autosomal dominant hearing loss by in vivo delivery of mini dCas13X-derived RNA base editor”的研究论文,该研究在肌球蛋白 VI p.C442Y 杂合突变 (Myo6C442Y/+ ) 小鼠模型(该模型概括了人类显性遗传性耳聋的表型)中使用基于 Cas13 的 RNA 碱基编辑器评估了 RNA 校正疗法。该研究首先在培养细胞中筛选了几种基于 Cas13 的 RNA 碱基编辑器和靶向 Myo6C442Y 的引导 RNA (gRNA),发现基于迷你 dCas13X.1 的腺苷碱基编辑器 (mxABE)[由截短的 Cas13X.1 和作用于 RNA 2 脱氨酶结构域变体 (ADAR2ddE488Q) 的 RNA 编辑酶腺苷脱氨酶组成],表现出高效率的 A > G 转换和低频率的脱靶编辑。
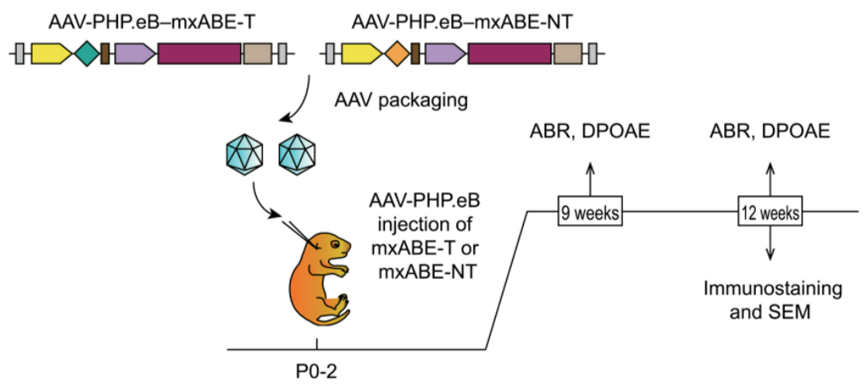
单个腺相关病毒 (AAV) 介导的 mxABE在耳蜗中的递送将突变的 Myo6C442Y 等位基因纠正为 Myo6WT (Myo6C442Y/C442Y)等位基因,并导致 Myo6C442Y/+ 小鼠的注射耳蜗中的 Myo6WT 等位基因增加。在向 Myo6C442Y/+ 小鼠注射 AAV-mxABE-Myo6 后长达 3 个月,该治疗挽救了听觉功能,包括听觉脑干反应等。该研究还观察到与未处理的对照耳相比,处理后的毛细胞存活率增加,毛束形态退化减少。总之,该研究结果支持将RNA 编辑治疗策略用于半显性疾病和潜在的隐性疾病。
另外,2022年4月26日,复旦大学附属眼耳鼻喉科医院舒易来主任、李华伟教授和陈兵教授团队合作在生物医学领域期刊Molecular Therapy-Nucleic Acids 在线发表了题为“Specific knockdown of Htra2 by CRISPR-CasRx prevents acquired sensorineural hearing loss in mice”的研究论文,该研究以基于CRISPR-CasRx 的RNA基因编辑前沿技术对药物引起的后天性感音神经性耳聋成功干预,为CasRx技术在临床的应用提供了重要理论依据。
2022年2月23日,复旦大学舒易来,李华伟,中国科学院上海神经科学研究所杨辉及中国农业科学院左二伟合作在Cell Research 在线发表题为“Treatment of autosomal recessive hearing loss via in vivo CRISPR/Cas9-mediated optimized homology-directed repair in mice”的研究论文,该研究基于同源介导的末端连接 (HMEJ) 的策略,修复了小鼠(Klhl18lowf 小鼠)常染色体隐性听力损失障碍。该研究的概念验证结果显示了进一步开发基于 HMEJ 的策略来修复导致遗传性听力损失以及其他人类遗传疾病的点突变的希望。