限时进食 (TRF) 最近作为一种潜在的抗衰老治疗方法引起了人们的兴趣,从果蝇到人类。TRF 将食物摄入量限制在一天中的特定时间。由于 TRF 控制进食时间,而不是营养或热量含量,因此假设 TRF 取决于昼夜节律调节功能;其作用的潜在分子机制仍不清楚。近期,美国哥伦比亚大学Mimi Shirasu-Hiza团队在Nature 在线发表题为“Circadian autophagy drives iTRF-mediated longevity”的研究论文,该研究为了利用果蝇的遗传工具和充分表征的衰老标志物,开发了一种间歇性TRF (iTRF) 饮食方案,可显著延长果蝇的寿命并延迟肌肉和肠道中衰老标志物的出现。
此外,该研究还发现禁食的时间对于延长寿命至关重要,只有在晚上禁食或午餐前后开始禁食寿命才会延长。白天禁食,晚上进食则没有帮助。该研究发现 iTRF 增强了昼夜节律调节的转录,并且 iTRF 介导的寿命延长需要昼夜节律调节和自噬,这是一种保守的长寿途径。夜间特异性自噬诱导对于延长随意饮食的寿命是必要和足够的,并且还阻止了 iTRF 介导的进一步寿命延长。相比之下,特定时间段的自噬诱导并没有延长寿命。因此,这些结果表明昼夜节律调节的自噬是 iTRF 介导的果蝇健康益处的关键因素。由于昼夜节律调节和自噬都是人类衰老过程中高度保守的过程,这项工作强调了刺激昼夜节律调节自噬的行为或药物干预可能为人们提供类似的健康益处,例如延缓衰老和延长寿命的可能性。
间歇性禁食是一种近年来流行的间歇性进食方式的统称,包括在一个期间内进行的断食与进食循环,研究发现间歇性断食是减少热量摄取,减轻体重,减少体脂肪量及改善胰岛素敏感性的可行策略。间歇性禁食通常分为两类:一种是每日限时进食(Time-restricted feeding),即将进食时间段缩窄至6到8小时;另一种是所谓的“5∶2间歇性禁食”,即每周7天中有两天仅吃一顿中等量的餐食。
一系列动物研究和人类研究表明,禁食与进食之间的交替有助于细胞健康,可能是通过触发一种代谢转换,即古老的应对食物短缺时期的适应方式。当细胞耗尽能快速获取基于糖的能量储备,并开始以较慢的代谢过程将脂肪转化为能量时,就会发生这种转换。
对不同物种的间歇性禁食的研究一致报告了许多健康状态的改善,即使没有减少卡路里摄入量。人类间歇性禁食的好处包括腹部脂肪减少和葡萄糖代谢、血压、心率变异性和身体耐力的改善。此外,在人类中观察到的热量限制对新陈代谢、器官功能和疾病抵抗力的几个主要积极影响可以通过间歇性禁食来概括,并且可以与体重减轻和总热量摄入的影响分开。限时进食和其他类型的间歇性禁食计划是生活方式干预措施,可以在全球范围内适用,从而以真正平等的方式使人们受益。但必须首先了解限时进食时间表如何促进健康和延长寿命。

果蝇进食干预策略(图源自Nature )
该研究对能够延长果蝇寿命的限时进食策略进行了筛选,发现果蝇从早晨中段开始,每隔一天禁食20小时,禁食日之间的恢复日果蝇可随意饮食,该策略相比其他饮食干预模型(全天自由进食;日间12h进食-夜间12h饥饿交替进行;24h饥饿与1-2天自由进食交替进行)能够显著延长非衰老果蝇的寿命(雌性果蝇的寿命延长了18%,雄性果蝇的寿命也延长了13%),该策略被称为间歇性 TRF (iTRF) 饮食方案。另外,iTRF 不仅可以延长寿命,还可以防止肌肉、神经元和肠道功能随着年龄的增长而下降。
禁食20小时的时间是至关重要的,只有在晚上禁食或午餐前后开始禁食的果蝇,寿命才会延长。白天禁食,只在晚上进食的果蝇的寿命没有改变。
该研究发现 iTRF 增强了昼夜节律调节的转录,并且 iTRF 介导的寿命延长需要昼夜节律调节和自噬,这是一种保守的长寿途径。夜间特异性自噬诱导对于延长随意饮食的寿命是必要和足够的,并且还阻止了 iTRF 介导的进一步寿命延长。相比之下,特定时间段的自噬诱导并没有延长寿命。

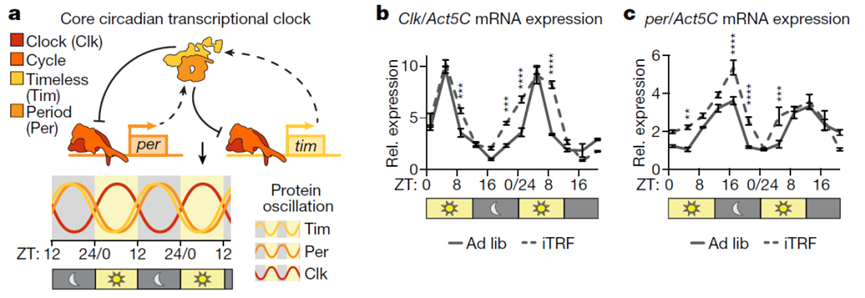
核心生物钟组件是iTRF介导的寿命和健康寿命延长所必需的(图源自Nature )
因此,这些结果表明昼夜节律调节的自噬是 iTRF 介导的果蝇健康益处的关键因素。由于昼夜节律调节和自噬都是人类衰老过程中高度保守的过程,这项工作强调了刺激昼夜节律调节自噬的行为或药物干预可能为人们提供类似的健康益处,例如延缓衰老和延长寿命的可能性。